딥러닝으로 신약 후보 물질을 짧은 기간 내에 디자인할 수 있다는 것을 증명한 논문이 최근 화제가 되었습니다. 이번 달 Nature Biotechnology에 실린 논문인데요. DDR1이라는 fibrosis (섬유증)에 관여하는 receptor tyrosine kinase를 저해할 수 있는 저분자 화합물을 디자인하는 연구였습니다. 특히 이런 분야의 논문으로는 극히 드물게도, 이 기술로 만들어낸 신약 후보 물질로 cell-based assay에서 inhibition 효과가 실제로 있음을 보여줬으며, rodent model 에서 pharmacokinetics 까지 보여주었습니다.
이 연구는 인공지능 신약 개발 스타트업 중에서는 꽤 이름이 알려진 Insilico Medicine의 연구자들이 주도하였습니다. 기본적으로 딥러닝의 일종인 강화학습(reinforced learning)을 사용한 GENTRL 이라 이름 붙인, deep generative model을 만들었습니다. 이 모델에는 DDR1과 기존에 알려진 저분자 화합물 DB 등을 학습시켰는데, 이를 이용하여 새로운 저분자 화합물의 구조를 도출하게 됩니다. 이를 실제로 합성해서 실험으로 증명한 것입니다.
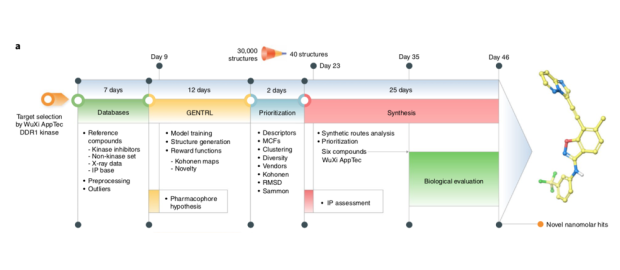
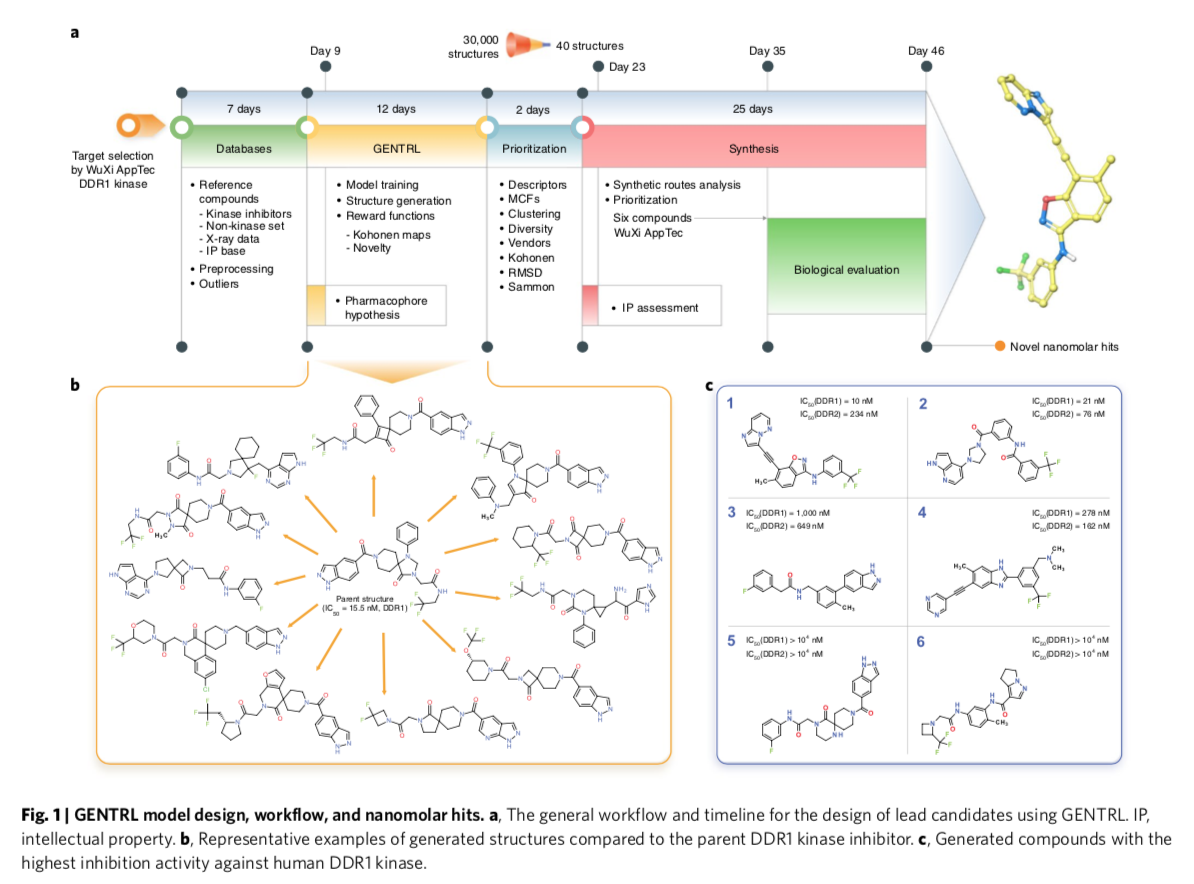
특히 이러한 과정을 시행한 시간대가 인상적입니다. 자신들이 만든 모델을 돌려서 단 21일만에 30,000여 개의 저분자 화합물을 디자인했습니다. 이 중에서 몇몇 기준을 바탕으로 (안정적이지 않은 구조이거나, 현재 상업적으로 판매되고 있는 화합물 구조와 너무 유사한 것들을 제외하는 등), chemical space를 최대한 커버할 수 있는 40개의 저분자 화합물 구조를 무작위로 선택하였습니다. 그리고 그 중에서 6개를 합성하는데 성공합니다. 여기까지 걸린 시간이 단 35일 입니다.
이 6개의 후보 물질이 in vitro에서 DDR1 inhibition activity를 보았더니, 1, 2번 두 개의 화합물은 strong inhibition (IC50이 각각 10nM, 21nM 까지 나옵니다!), 3, 4번 두 개는 moderate potency (IC50가 1nM, 278nM), 그리고 나머지 두 개는 inactive 였습니다.
이어서, 1, 2번 화합물은 U2OS cell, LX-2 cell 에서 fibrotic marker 여러 가지를 효과적으로 inhibition함을 확인하였습니다. 얘네들은 half-life와 clearance 도 control molecule과 비슷하게 나왔으며, 더 나아가서 1번은 rodent model 에서 iv, orally 주입해봤더니 둘 다 half life는 3.5h 정도임을 보여주었습니다.
아니나 다를까, 1번 화합물은 molecular docking simulation을 해보았더니, DDR1의 ATP binding site와 잘 맞아떨어집니다. H-bond 도 만드는 것 같고, charge, hydrophobic interaction 등도 이 active site와 잘 맞는 것 같습니다. 이렇게 타겟 사이트에 잘 결합하기 때문에 inhibition effect가 potent 하게 나오는 것으로 추정해볼 수 있습니다.
이러한 논문 이후에 중요 한 것은 두 가지 정도일 것 같습니다.
1. 이렇게 찾은 저분자 화합물이 이어진 임상에서도 좋은 성과를 낼 것인가. 사실 이번 논문에서는 저분자 화합물 2개만(?) 강한 저해 효과를 보인다고 했지만, 이러한 방법이 성공적이었으므로, 더 스케일을 키워서 더 많은 선도 물질을 찾아낼 수 있을 것입니다. 이를 이용해서 동물 모델에서 이 화합물이 어떠한 성과를 보이는지를 검증해봐야 하겠습니다. 특히 이번 논문에서는 강하게 결합한다, 세포 수준에서의 효과를 보여준 정도이므로, 동물 모델에서 효능이나 ADMET이 어떻게 나오는지는 추가적으로 검증해야 할 것입니다.
2. 어쩌면 더 중요하게도, 이러한 기술이 DDR1이 아닌 다른 표적에도 범용적으로 적용될 수 있는 기술이냐 하는 것입니다. 이번 강화학습 모델을 만들기 위해서 포함된 학습 데이터 중에는 기존에 알려진 DDR1 kinase inhibitor 들이나, DDR1의 3차 구조 등이 포함됩니다. 이러한 데이터가 모든 표적 단백질에 대해서 사용 가능한 것은 아니므로, 다른 표적에 대해서는 적용이 어쩌면 어려울 수도 있습니다. 다만 논문 내에서 여기에 대한 언급은 그리 많지 않고, 결국 추가적인 연구가 필요할 것으로 보입니다.


![[논문] LLM이 의료 전문가보다 의학 텍스트 요약을 더 잘 한다](https://www.yoonsupchoi.com/wp-content/uploads/2024/03/Untitled-8-140x90.png)
![[영상] 카카오 브레인의 배웅 최고 헬스케어 책임자(CHO) 님 인터뷰](https://www.yoonsupchoi.com/wp-content/uploads/2024/03/배웅-부사장님-140x90.jpg)
![[공지] DHP 디지털 헬스케어 아카데미 2024 (6기)의 수강생을 모집합니다!](https://www.yoonsupchoi.com/wp-content/uploads/2024/02/홈페이지-메인배너-이미지-copy-140x90.jpg)

















