Foundation Medicine은 현재 세계적으로 손꼽히는 암 유전체 의학의 아이콘 중 하나이자, 일반 환자 대상으로 암 유전체 테스트를 최초로 상용화 한 기업입니다. 전 세계 관련 기업들로부터 벤치마킹의 대상이 되고 있는 이 Foundation Medicine은 미국에서 암 환자 대상의 유전체 분석 서비스를 차근차근 확대해 나가고 있습니다.
유전체 분석이 세계적 암 표준 치료법인 NCCN 가이드라인에 포함되는가 하면, 미국의 의료 보험사는 FoundationOne 테스트에 의료 보험을 적용하기로 하였습니다. 또한, Foundation Medicine은 여기에 그치지 않고 FoundationOne 테스트를 받은 환자의 장기 예후 추적을 통한 비용효과성을 증명하여 보험 적용을 더 확대하려 하고 있습니다. 또한 구글은 전 직원과 직원의 가족들이 암에 걸릴 경우 FoundationOne 테스트를 무상으로 제공하기로 하였습니다.
이번 포스팅에서는 이와 같이 최근에 발표된 Foundation Medicine 및 암 유전체 의학에 관한 새롭고도 중요한 소식들을 조금 정리해보려 합니다.
암 유전체 의학의 아이콘, Foundation Medicine
암 환자의 유전체 분석을 바탕으로 최적의 치료법을 찾아주는 Foundation Medicine에 대해서는 제가 블로그와 책 등에서 여러 번 언급해드린 적이 있습니다. 이 회사는 휴먼 게놈 프로젝트를 주도한 브로드 연구소(Broad Institute)에서 2010년 스핀오프한 바이오 벤처입니다. 암 환자의 생검(biopsy)을 통해 얻은 FFPE 시료 (암세포를 파라핀으로 고정시킨 것) 를 통해 암 세포의 DNA를 분석하여, 암을 발병시킨 원인 유전자 (driver mutation)의 후보들을 골라줍니다.
현재 상용 출시된 암 유전체 검사들 중에 가장 종합적인 테스트라고 자타공인 받고 있습니다. 이 회사는 크게 두 가지의 분석 서비스를 제공합니다.
- 첫번째로 FoundationOne은 유방암, 폐암, 대장암 등의 고형암에 대해서 315개의 유전자 전 영역, 및 28개 유전자의 인트론(intron) 영역을 검사해줍니다. 테스트의 가격은 $5,800 입니다.
- 2013년 12월에 MSKCC와의 협력을 통해서 새롭게 출시한 FoundationOne Heme는 혈액암 대상의 테스트로 405 유전자의 DNA와 265개 유전자의 RNA를 검사합니다. 가격은 $7,200 입니다.
이 테스트의 결과로는 발견한 원인 유전 변이 중에, 치료 가능한 변이 (actionable mutation) 및 이에 사용할 수 있는 표적 치료제를 추천해줍니다. 특이할 점은 환자가 걸린 암에 대해 승인 받은 치료제 분만 아니라, 다른 암에 승인 받았으나 동일한 유전 변이를 표적으로 하는 치료제 및 현재 임상 시험 중인 치료제 까지도 추천해줍니다.
아래의 그림은 실제 FoundationOne의 결과 보고서 중 일부를 나타낸 예시입니다. 이 사례에서는 폐선암 (lung adenocarcinoma) 환자에게 검사한 결과를 보여주고 있으며,
- EGFR이라는 유전자에 암을 발병시킨 원이로 추측되는 변이가 발생하였습니다.
- 이 유전자(에서 나오는 단백질)을 표적으로 하면서, 폐선암에 승인 받은 약은 Erlotinib과 Gefitinib이 있으며,
- EGFR을 표적으로 하지만, 다른 폐선암 외의 암종에 승인을 받은 약은 Cetuximab과 Panitumumab이 있습니다.
- 또한 EGFR을 표적으로 하는, 임상시험 중에 있는 약도 있음을 알려줍니다.
종양내과 의사는 병리과에 의뢰하여 자기 환자의 FFPE 시료를 Foundation Medicine에 보낸 뒤, 2-3주 후면 온라인으로 이러한 형태의 보고서를 받아볼 수 있습니다. 이를 기반으로 해당 환자에 대한 의학적인 의사결정을 내리는 것입니다.
 FoundationOne 테스트 결과 레포트의 예시
FoundationOne 테스트 결과 레포트의 예시
제가 예전에 올려드린 ‘스티브 잡스가 암 맞춤 치료에 남기고 간 것들‘에서도 알려드린 바 있듯이, 스티브 잡스도 작고하기 몇달 전 아직 출시 전이던 FoudationOne의 프로토타입 형태의 테스트를 받았던 것으로 화제를 모으기도 했습니다. 잡스의 경우, 이상 유전 변이는 찾을 수 있었으나, 그 변이에 대한 치료제가 없었던 것으로 알려져 있습니다.
유전체 검사 NCCN 가이드라인에 포함
이러한 유전체 의학은 한국과는 달리 미국에서는 점차 확대되어 가고 있습니다. 올해 들어 아마도 암 유전체 의학계의 가장 중요한 뉴스 중의 하나는 미국의 NCCN (National Comprehensive Cancer Network, 국립종합암네트워크) 가이드라인에 유전체 분석이 정식으로 포함되었다는 것으로 보입니다. NCCN 가이드라인은 암을 치료하기 위한 일종의 국제 표준 치료법 권고안으로, 전세계의 병원 및 종양학자들에게서 널리 받아들여지며, 보험급여의 기준으로도 참고되고 있습니다.
이 NCCN 가이드라인은 과학 기술의 발전을 참고하여 정기적으로 가이드라인을 업데이트 하고 있으며, 드디어 2014년 버전에 유전체 분석이 최초로 표준 검사 방법에 포함된 것이었습니다. 비세포성 폐암 (Non-small cell lung cancer) 4기 환자를 대상으로는 차세대 서열 분석 (NGS, Next Generation Sequencing) 등을 통한 EGFR, ALK 유전자의 검사를 권고한 것입니다. 유전체 분석이 표준 가이드라인에 포함된 것은 전체 암종을 통틀어서 이것이 최초입니다.
 비세포성폐암(Non-Small Cell Lung Cancer)의 NCCN 가이드라인에
비세포성폐암(Non-Small Cell Lung Cancer)의 NCCN 가이드라인에
Next-generation sequencing 이 포함되어 있습니다
이에 따라 미국에서는 폐암을 시작으로 암 유전체 분석이 더욱 확대되고 있는 것 같습니다. 아직 한국은 유전체 서열 분석기기 및 시약이 아직 식약처 허가를 받지 않아서 사용이 불가합니다. 하지만, 미국의 경우 작년에 일루미나의 MiSeqDx 기기 및 시약이 FDA 승인을 받았으며, 한국과는 다르게 개별 연구실 수준에서 개발한 임상 테스트 (Labratory Developed Test, LDT) 도 일정 기준을 충족시키기만 하면 상용화가 가능합니다. Foundation Medicine도 대표적인 LDT 유형의 서비스 제공자 중의 하나이며, 이러한 NCCN 가이드라인 업데이트를 통한 유전체 분석 확대의 수혜를 입고 있다고 할 수 있습니다.
의료 보험사 Priority Health, FoundationOne 테스트 지원
더 많은 암 환자들이 Foundation Medicine 이 제공하는 서비스를 받게되는 계기가 될 뉴스는 또 있습니다. 지난 10월 16일에는 Priority Health라는 미국의 의료 보험사는, 보험사로서는 최초로 가입자가 암에 걸렸을 경우 FoundationOne 테스트를 지원하겠다고 발표한 것입니다. 사실 지금까지도 환자들은 Foundation Medicine의 테스트에 대해서 보험금을 지급 받곤 했습니다. (약 $6,000-7,000의 테스트 비용 중 평균적으로 $3,000 정도를 지원 받은 것으로 알려져 있습니다)
하지만 과거에는 개별 환자 케이스마다 개별적으로 보험사와 협상을 해야 했던 반면, Priority Health는 60만 명 이상의 보험 가입자 전원을 대상으로 혜택을 제공하기로 했다는 점이 큰 차이입니다. 사실 암 환자로서는 목숨이 걸려 있지만, 수천 불이나 하는 테스트가 금전적으로 전혀 부담이 없을 수는 없습니다. 만약 보험사의 FoundationOne 테스트 비용을 지원이 확대된다면, 이 테스트는 더욱 빠르게 확산될 수 있을 것입니다.
환자의 장기 모니터링을 통한 비용효과성 증명
여기에서 그치지 않고, Foundation Medicine은 의료 보험 혜택을 받는 암 환자의 비율을 늘리기 위해서 보다 적극적으로 준비하고 있습니다. 이 회사는 FoundationOne 테스트를 받은 환자들의 치료 결과 및 소요된 비용 등을 장기적으로 추적 관찰하기 위해서 Cancer Outcomes Tracking and Analysis (COTA)와 파트너십을 맺었습니다.
COTA는 클라우드를 기반으로 암 환자의 유전 정보 등의 데이터를 수집하여 해당 환자의 암을 세부적으로 분류하고, 환자의 예후를 추적하며 종양내과 의사에게 유의미한 보고를 실시간으로 제공하는 서비스입니다. 유투브 동영상 캡쳐인 아래 그림을 보면 유방암 환자를 병기, 조직, 전이 정도, ER, PR, Her2, BRCA 등 주요 마커들의 양성/음성을 기준으로 세부적으로 분류합니다. (사실 이 정도 분류는 아주 일반적인데… 실제로는 내부적으로 사용하는 좀 더 세부적인 분류법이 있을 것 같습니다) 종양내과 의사들 주도로 만들어진 스타트업이며, 최근에 시리즈 A 펀딩에 성공하였습니다.
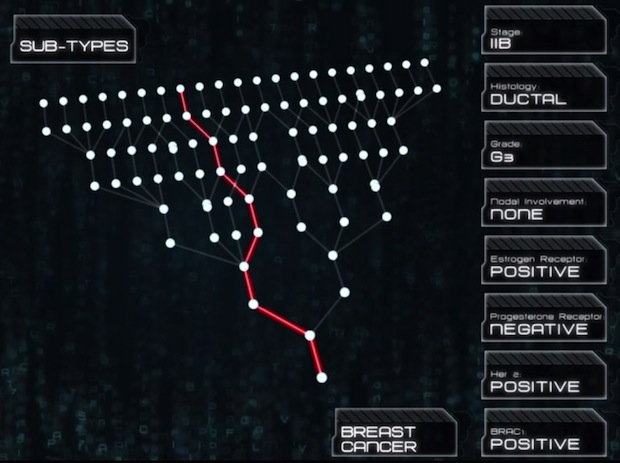 COTA (출처: 유투브)
COTA (출처: 유투브)
Foundation Medicine과 COTA 는 지난 11월 4일 체결한 이 파트너십을 통해서, FoudationOne 테스트를 받은 비세포성 폐암(NSCLC) 4기 환자 (즉, NCCN 가이드라인에서 유전체 분석의 표준 치료법 권고의 대상이 된 바로 그 암종과 병기) 를 대상으로 유전체 데이터, 임상 정보 및 치료 결과, 경제성 데이터 등을 축적하기로 하였습니다.
이러한 데이터는 추후 보험사를 대상으로, 폐암 환자에 대한 유전체 분석 테스트의 효용성 및 비용 효용성 (cost-effectiveness) 을 정량적으로 증명함으로써 의료 보험의 범위를 더 확대하기 위한 근거로 쓰일 것입니다. 회사 측은 임상 의사들과 연구자들도 이 데이터로부터 많은 인사이트를 얻을 것으로 기대하고 있습니다.
흔히 항암제는 암 한자의 다형성 (heterogeneity) 등 때문에 실제 약효가 있는 약이 25%에 그친다고 이야기 합니다 (아래 그림 참조). 이 때문에 환자의 치료 성과 측면 뿐만 아니라, 의료비의 낭비 부분도 지적되어 왔습니다. 유전체 검사를 통해서 ‘최적’의 치료제를 선택함으로써 의료비를 절감할 가능성이 크지만, 유전체 검사 자체가 현재 수천불 수준의 비용이 소요되기 때문에 비용효과성을 측정하기가 쉽지 않습니다.
이 때문에 비용 효용성을 검증하기 위해서는 일정 규모 이상의 유전체 의학 검사를 받은 환자들을 대상으로 장기간 추적 연구가 필요합니다. 이를 Foundation Medicine은 COTA와 함께 하겠다는 것으로 보입니다. FoundationOne 테스트를 통해서 장기적으로 불필요한 처방, 부작용을 줄이고, 최적의 항암제를 선택함으로써 비용효과성(cost-effectiveness)를 증명할 수 있다면, 의료 보험의 범위를 더욱 확대하기 위한 근거로 적극적으로 활용될 수 있을것입니다.
NCCN 가이드라인에도 포함된 표준 검사가, 의료 보험의 혜택도 받게 된다면 암 유전체 의학은 아주 일상적인 암 환자 진료 프로세스 속으로 빠르게 편입될 것입니다.
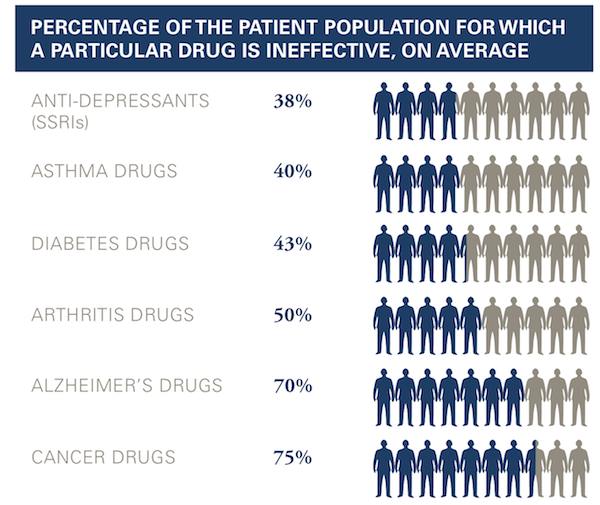 평균적으로 항암제 중 75%가 약효가 ‘없음’
평균적으로 항암제 중 75%가 약효가 ‘없음’
구글, 직원에게 FoundationOne 테스트를 무상 제공
그런가 하면, 지난 11월 5일 구글은 자사의 직원과 직원의 가족들이 암에 걸렸을 경우 FoundationOne 테스트를 2015년부터 무상으로 제공하겠다고 발표했습니다. 작년 9월 나스닥 시장에 상장한 Foundation Medicine에 설립 초기부터 투자를 했던 곳이 다름아닌 Google Ventures 였습니다. Google Ventures는 2011년 시리즈 A 펀딩과 2012년 시리즈 B 펀딩에도 참여했습니다. 총 $13m 을 투자했던 구글의 지분 가치는 Foundation Medicine의 상장 당시 $90m 으로 상승하기도 했습니다.
뿐만 아니라, 구글은 Foundation Medicine이 의사에게 웹을 통해서 분석 결과를 제공하는 Interactive Cancer Explorer 인터페이스를 구축할 때도 도움을 주기도 했다고 알려져 있습니다.
이제 구글은 단순히 재무 투자나 프로그램 개발이 아니라, Foundation Medicine의 상품을 자사의 직원들을 위해서 적극적으로 활용하기로 한 것입니다. 미국의 대표적인 거대 기업 중 하나인 구글이 46,000명에 달하는 자사의 직원들을 대상으로 이러한 서비스를 제공하기로 한 것도 의미 심장하게 보입니다. Foundation Medicine의 암유전체 의료 테스트에 대한 구글의 신뢰, 그리고 미국 내에서 암 유전체 의학이 얼마나 널리 사용되기 시작했는지를 단적으로 보여준다고 하겠습니다.

LDT 규제와 새로운 경쟁자의 진입
사실 Foundation Medicine의 앞날은 밝기만 한 것은 아닙니다. 지난 7월 FDA가 지금까지는 거의 규제 받지 않던, 실험실 내부 개발 테스트 (LDT, Laboratory-Developed Test)를 향후 규제하겠다고 밝힌 것입니다. 미국에서 40여년 전 부터 시행되어 온 LDT는 주로 체외 진단 테스트가 주를 이루었으며, 과거에는 개별 병원 수준에서 비교적 복잡하지 않은 검사를 수행하기 위한 목적으로 사용되었습니다. 이러한 테스트가 숙련된 전문가들에 의해서 정확한 결과를 내어놓고, CLIA (Clinical Laboratory Improvement Amendments) 라는 규정을 준수한다면, FDA는 별다른 규제/승인 절차 없이도 서비스를 허용했습니다.
하지만 최근에 이러한 LDT는 대형 병원이나 연구 기관들에 의해서 단순히 한 병원 뿐만 아니라, 미국 전역을 대상으로 한 서비스로 확대되었습니다. 그 대표적인 분야가 암 맞춤 의료이며, 그 분야의 필두가 바로 Foundation Medicine 입니다. FDA는 이러한 기존의 진단 기기들이 받던 기준에 상응하는 규제를 적용할 것으로 발표했습니다. Foundation Medicine도 향후 이러한 규제를 거쳐야 할 것으로 보입니다. (LDT 규제의 배경은 여기에 잘 설명되어 있습니다)
또한 경쟁자들의 시장 진입도 Foundation Medicine으로는 걱정 거리 중의 하나입니다. (암 환자들은 더 환영할 뉴스로 보입니다) 세계 유전체 서열 분석 기기 시장을 장악하고 있는 일루미나(Illumina)는 지난 8월 다국적 제약사 아스트라제네카, 얀센, 사노피와의 협력을 통해서 유전체 분석 기반의 항암제 동반 진단 시장에 진출할 것을 발표한 것입니다.
일루미나는 작년 FDA로부터 MiSeqDx 라는 서열 분석 기기에 대해 세계 최초로 의료용 승인을 받았으며, 올해 초에는 HiSeq X Ten 이라는 새로운 기기를 내어놓으며 ‘$1,000 게놈’ 시대를 견인한 장본인입니다. 특히, Foundation Medicine도 일루미나의 기기를 사용하는 것으로 알려져 있습니다. 유전체 서열 분석 기기 시장을 장악하고 있는 일루미나가, 가치 사슬(value chain) 상에서 바로 뒷단에 있는 유전체 분석 기반 진단 시장으로 사업을 확장하는 것은 매우 자연스럽고도 당연한 전략으로 보입니다.
일루미나가 개발하기로 한 동반진단기기 (CDx, Companion Diagnostics)는 특정 표적 치료제의 처방 여부를 결정하기 위해서, ‘동반되는’, 혹은 ‘공식적으로 짝지어진 진단 기기라고 할 수 있습니다. 암 환자가 특정 유전 변이를 가지고 있는지의 여부를 판단하기 위해서 검사한다는 점은 Foundation Medicine과 동일합니다. 하지만 아마도 CDx는 ‘임상적 검증성 (clinical validity)’ 까지 확인하여, ‘이 진단에서 나온 약을 사용하면, 반드시 약효가 있다’는 것까지 증명하게 될 것 같습니다. Foundation Medicine으로서는 별로 달갑지 않은 뉴스임에 분명합니다.
Foundation Medicine과 암 유전체 의학의 미래
최근 Foundation Medicine의 실적은 나날이 좋아지고 있습니다. 최근 발표한 2014년 3사분기 실적을 보면 해당 분기에만 6,428 번의 테스트를 서비스 하며 전년 동기 대비 149%의 성장을, 매출은 $16.4m 을 기록하며 전년 동기 대비 100%의 성장을 이뤄내고 있습니다. 특히 환자들을 대상으로 한 서비스의 매출이 $9.8m, 제약회사를 대상으로 한 매출이 $6.7m 으로 고루 분포되어 있습니다. 올해 총 매출은 연초 제시한 $52m-58m에서 $58m-60m 으로 상향 조정되었으며, 올해 제공한 총 테스트의 수는 22,000-25,000 건으로 예상하고 있습니다.
세계 암 유전체 의학의 대표 주자인 Foundation Medicine은 이렇게 서비스 판매를 확대하고 있습니다. 뿐만 아니라, NCCN 가이드라인 포함 및 의료 보험 혜택 확대 등의 환경적인 요인까지 개선되어 가는 것을 알 수 있습니다. 반면 LDT 규제와 경쟁자의 진입 등의 위험 요소도 도사리고 있습니다.
Foundation Medicine이 앞으로 이러한 조건 속에서 어떠한 성과를 거둬들일지 기대됩니다. 분명한 것은 암 유전체 의학의 발전은 계속되고 있다는 점이고, 이에 혜택을 받는 암 환자들은 더욱 늘어날 것이라는 점입니다. 한국의 암 환자들도 하루 빨리 이러한 암 유전체 의학 발전의 혜택을 얻을 수 있기를 바랍니다.






















1 Comment